Тирзепатид: Двоен GIP/GLP-1 агонист
Механизъм, клинично превъзходство и протоколи
Въведение
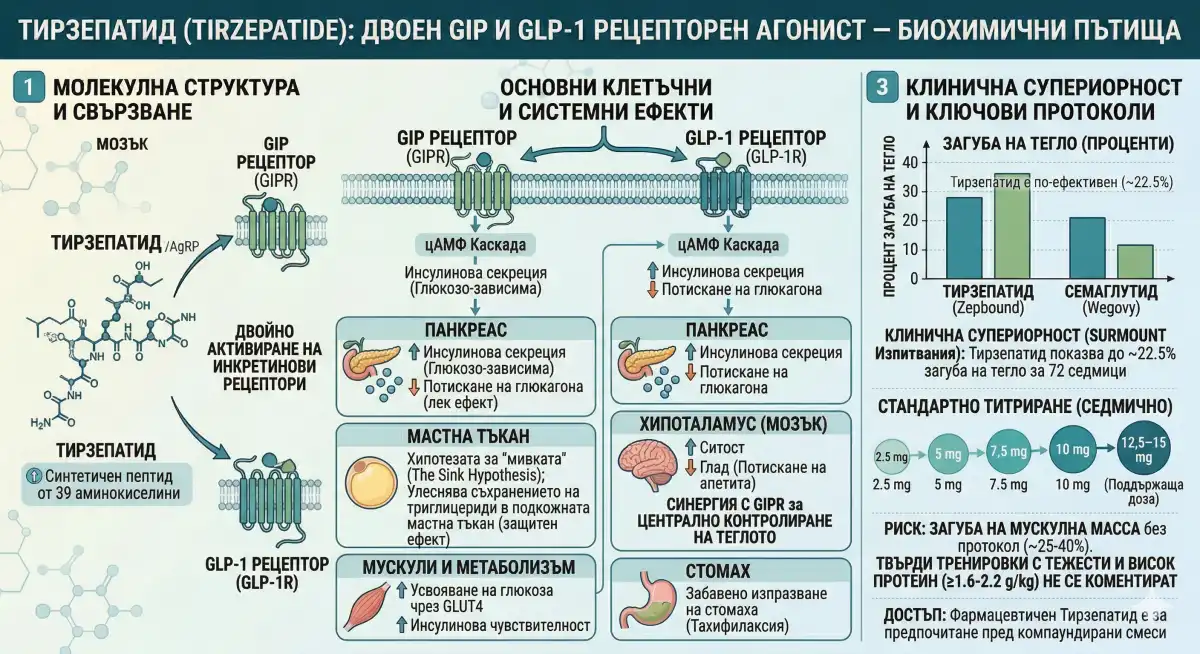
Тирзепатид (предлаган на пазара като Mounjaro за диабет тип 2 и Zepbound за затлъстяване) е първият одобрен двоен инкретинов рецепторен агонист — единичен пептид от 39 аминокиселини, който едновременно активира рецепторите на глюкозо-зависимия инсулинотропен полипептид (GIP) и глюкагоноподобния пептид-1 (GLP-1). Докато семаглутид открехна вратата към фармакологичната загуба на тегло, тирзепатид я разби напълно. В директни клинични изпитвания той постоянно превъзхожда агонистите само на GLP-1 както по отношение на намаляването на теглото, така и по отношение на гликемичния контрол, произвеждайки 15–26% загуба на общо телесно тегло в клинични изпитвания при хора — цифри, които се доближават до територията на бариатричната хирургия без скалпел.
За общността на биохакинга и самооптимизацията тирзепатид представлява най-мощният фармакологичен инструмент за загуба на тегло и метаболитен контрол, наличен в момента. Но неговият механизъм е по-нюансиран от "по-силен Ozempic", а практическите съображения — титриране, странични ефекти, запазване на мускулите, цена и почти сигурното възвръщане на теглото при спиране — изискват ясен и обективен анализ.
Биохимичен механизъм: Защо два рецептора са по-добри от един
Агонизъм на GLP-1 рецептора
Компонентът на GLP-1R работи чрез добре установени пътища. Активирането на GLP-1 рецепторите върху POMC/CART невроните в аркуатното ядро на хипоталамуса стимулира анорексигенно (потискащо апетита) сигнализиране. Периферно, активирането на GLP-1R върху бета-клетките на панкреаса засилва стимулираната от глюкозата секреция на инсулин, забавя изпразването на стомаха и потиска освобождаването на глюкагон. Това е същият основен механизъм, експлоатиран от семаглутид и лираглутид.
Агонизъм на GIP рецептора — Спорният усилвател
Ролята на GIP във фармакологията на затлъстяването исторически се е смятала за парадоксална. Известно е, че GIP насърчава съхранението на триглицериди в адипоцитите — което изглежда контрапродуктивно за лекарство за загуба на тегло. Възникващият модел, подкрепен от предклинични данни, преформулира това:
- Хипотезата за "мивката" (The "Sink" Hypothesis): Медиираното от GIP съхранение на триглицериди в адипоцитите може да функционира като метаболитен шънт, насочващ липидите към подкожната мастна тъкан (метаболитно по-безопасна) и далеч от ектопични депа като черния дроб и вътрешностите (Heise et al., 2022).
- Синергия в ЦНС: GIPR се експресира върху хипоталамичните неврони, включително същите POMC/CART популации, насочени от GLP-1. GIP преминава кръвно-мозъчната бариера по-лесно от GLP-1 и се предполага, че съвместното активиране усилва вътреклетъчното cAMP сигнализиране, предизвиквайки потискане на апетита, по-голямо от всеки от пътищата поотделно (Secher et al., 2014; Frias et al., 2021 — модели на гризачи).
- Анти-тахифилактичен ефект: Може би най-убедителната хипотеза е, че агонизмът на GIPR предотвратява контрарегулаторната регулация надолу, която отслабва ефектите от хроничната терапия само с GLP-1. Това би обяснило постоянното и разширяващо се разделяне на кривите за загуба на тегло между тирзепатид и семаглутид за над 72+ седмици в изпитванията.
Важно предупреждение: Механистичното обяснение за синергичната роля на GIP разчита до голяма степен на данни от животни и in vitro. Хипотезите за синергията в ЦНС и "мивката" са правдоподобни, но не са окончателно доказани при хора. Клиничното превъзходство е доказано; точното "защо" все още е със средна степен на увереност.
Ефекти върху бета-клетките на панкреаса
Двата рецептора се сближават върху бета-клетките. Активирането на GIPR увеличава вътреклетъчния cAMP, като увеличава стимулираната от глюкозата секреция на инсулин по глюкозо-зависим начин (Nauck et al., 2021 — механистично подпроучване SURPASS-2). Този двоен път осигурява по-физиологично нюансиран инсулинов отговор отколкото само GLP-1, като потенциално намалява риска от хипогликемия, докато постига превъзходен постпрандиален глюкозен контрол. Това са данни с висока степен на увереност при хора.
Периферни метаболитни ефекти
GIP насърчава усвояването на глюкоза в скелетната мускулатура чрез транслокация на GLUT4, докато активността на GLP-1 намалява ектопичните чернодробни мазнини. Комбинираният резултат: подобрена инсулинова чувствителност на цялото тяло и теоретична основа за запазване на мускулната маса по време на калориен дефицит (Thomas et al., 2023 — анализ на телесния състав в SURMOUNT-1; Heise et al., 2022 — индиректна калориметрия).
Данни от клинични изпитвания: Числата
Изпитвания SURMOUNT (Затлъстяване)
Програмата SURMOUNT установи доминацията на тирзепатид във фармакотерапията на затлъстяването:
- SURMOUNT-1: Участниците без диабет тип 2 са постигнали зависима от дозата загуба на тегло от приблизително 15% (5mg), 20% (10mg) и 21–22,5% (15mg) от общото телесно тегло за 72 седмици.
- SURMOUNT-4: Демонстрира устойчива ~21% загуба на тегло на 88-мата седмица при продължаваща терапия — но критично, групата на кросоувър към плацебо показа значително възвръщане на теглото, потвърждавайки, че спирането води до възстановяване.
Изпитвания SURPASS (Диабет тип 2) — Директно сравнение със семаглутид
SURPASS-2 беше решаващото директно изпитване срещу семаглутид 1mg:
Метрика | Тирзепатид 15mg | Семаглутид 1mg |
|---|---|---|
Намаляване на A1c | −2,3% | −1,86% |
Загуба на телесно тегло | 11,2–13,0% | 6,2% |
Популация | Диабет тип 2 | Диабет тип 2 |
Тирзепатид удвоява загубата на тегло в сравнение със семаглутид в диабетна популация, като същевременно постига превъзходен гликемичен контрол. Това са стабилни резултати от изпитвания фаза 3 при хора — данни с висока степен на увереност.
Метаболитни подобрения отвъд теглото
Във всички програми за изпитвания тирзепатид демонстрира:
- Намаляване на A1c: До 2,3% (клинично масивно).
- Кръвно налягане: Значителни намаления, вероятно вторични от загубата на тегло.
- Липиден профил: Подобрения в триглицеридите и атерогенните липидни частици.
- Чернодробни мазнини: Съществено намаляване, като в момента се провеждат активни изпитвания за NASH/MASH (SYNERGY-NASH, резултати се очакват 2025–2026).
Протокол за дозиране и титриране
Стандартното клинично титриране е предназначено да управлява стомашно-чревната поносимост:
Седмица | Доза | Цел |
|---|---|---|
1–4 | 2,5mg QW (седмично) | Започване (субтерапевтична за загуба на тегло) |
5–8 | 5mg QW (седмично) | Първа терапевтична доза |
9–12 | 7,5mg QW (седмично) | Междинна стъпка |
13–16 | 10mg QW (седмично) | Силна терапевтична доза |
17+ | 12,5–15mg QW (седмично) | Максимална доза |
Приложението е подкожна инжекция веднъж седмично (корем, бедро или горна част на ръката). Постепенното титриране нагоре позволява на плътността на GLP-1R и GIPR и сигналните пътища надолу по веригата да се адаптират, като значително намалява честотата и тежестта на гаденето, повръщането и диарията.
Практически бележки за оптимизиращо настроените
- Минимална ефективна доза: Кривата доза-отговор между 5mg и 15mg е стръмна, но също такава е и кривата на стомашно-чревните странични ефекти. Намирането на индивидуалната минимална ефективна доза (напр. 7,5 mg или 10 mg) за устойчива загуба с поносими странични ефекти може да бъде по-практично от преминаването към 15 mg. Докладите от общността показват, че много потребители се стабилизират на 10 mg с отлични резултати.
- Време на инжектиране: Няма строго изискване, но последователността (в един и същи ден всяка седмица) е важна за стационарните нива.
- Дозиране с удължен интервал и микродозиране: Някои членове на биохакинг общността експериментират със субседмични или по-ниски от предписаните дози. Тези протоколи са изцяло анекдотични и нямат официални данни за безопасност или ефикасност.
Тирзепатид срещу Семаглутид: Практическо сравнение
Фактор | Тирзепатид (Mounjaro/Zepbound) | Семаглутид (Wegovy/Ozempic) |
|---|---|---|
Механизъм | Двоен GIP/GLP-1 агонист | Само GLP-1 агонист |
Молекулна структура | Пептид от 39 аминокиселини | 31-аминокиселини със странична верига от мастна киселина |
Максимална загуба на тегло (изпитвания) | 20–26% TBW (общо телесно тегло) | 15–17% TBW (общо телесно тегло) |
Намаляване на A1c | До 2,3% | До 1,86% |
Приложение | Седмична подкожна (SC) инжекция | Седмична подкожна (SC) инжекция |
Стомашно-чревни странични ефекти | Подобен профил, потенциално по-добре понасян при еквивалентна ефикасност поради титрирането | Добре характеризирани; гаденето е най-често срещано |
Данни за сърдечно-съдови резултати (CV) | Предстоящи (SURMOUNT-MMO, ~2027) | Доказана полза при диабет тип 2 (изпитване SELECT) |
Цена (САЩ) | ~$1,000+/месец | ~$1,000+/месец |
Най-добро за | Максимална загуба на тегло/Намаляване на A1c | Установена CV защита при диабет тип 2; по-широко застрахователно покритие |
Ключов извод: Ако целта е максимална загуба на тегло или гликемичен контрол и разходите/достъпът са управляеми, тирзепатид е по-силният инструмент. Ако намаляването на сърдечно-съдовия риск при диабет тип 2 е основният двигател, семаглутид има доказани данни за резултати (изпитване SELECT). Дългосрочните CV данни за тирзепатид при популации със затлъстяване без диабет няма да бъдат налични, докато не приключи SURMOUNT-MMO (~2027 г.).
Запазване на мускулната маса: Сигнал или шум?
Това е твърдението, което има най-голямо значение за фитнес общността — и доказателствата са обещаващи, но предварителни.
Анализът на телесния състав от SURMOUNT-1 (Thomas et al., 2023) предполага, че потребителите на тирзепатид са запазили по-висок дял чиста маса спрямо общото загубено тегло в сравнение с исторически данни само от калорийно ограничение. Предложеният механизъм: медиираната от GIP транслокация на GLUT4 в скелетните мускули насочва глюкозата към функционалната тъкан по време на калориен дефицит.
Въпреки това: Не е завършено рандомизирано контролирано изпитване, което директно да сравнява тирзепатид срещу семаглутид по отношение на резултатите за чистата маса с помощта на DEXA или ЯМР, като същевременно контролира приема на протеини и упражненията. Твърдението за запазване на мускулите остава в най-добрия случай със средна степен на увереност. За всеки, който използва тирзепатид в контекста на спортни постижения или телесен състав, стандартният съвет важи с допълнителна спешност:
- Тренировките с тежести (съпротивление) не подлежат на преговори.
- Прием на протеин ≥1,6 g/kg/ден (някои протоколи в общността достигат до 2,2 g/kg).
- Наблюдавайте телесния състав чрез DEXA, а не само чрез теглото на кантара.
Странични ефекти и управление
Чести (преходни, зависими от дозата)
- Гадене (най-често, обикновено достига връх при ескалация на дозата и отшумява).
- Диария и запек (могат да се редуват).
- Намален апетит (функция, а не бъг — но може да стане прекомерен).
- Реакции на мястото на инжектиране (леки).
Сериозни (редки, но реални)
- Панкреатит: Рядко; прекратете, ако се подозира.
- Заболяване на жлъчния мехур: Бързата загуба на тегло разкрива камъни в жлъчката. Рискът се увеличава при по-високи дози и по-бързи темпове на загуба.
- Медуларен карцином на щитовидната жлеза (MTC): Тумори на С-клетките, наблюдавани при проучвания с гризачи. Противопоказано при пациенти с лична или фамилна анамнеза за MTC или MEN2. Няма потвърден сигнал в клинични изпитвания при хора, но предупреждението в черна кутия остава валидно.
- "Лице на Mounjaro" (Mounjaro face): Лицева липодистрофия от бърза загуба на мазнини — козметично, не е опасно, но е забележимо.
Стратегии за управление
- Стриктно спазване на графика за титриране.
- По-малки, по-чести хранения.
- Избягване на ястия с високо съдържание на мазнини (изостря гаденето).
- Ондансетрон (Zofran) при необходимост за гадене, ако е тежко.
- Ако е непоносимо при дадена доза, задръжте на предишната доза за допълнителни 4 седмици, преди да опитате отново ескалация.
Регулаторен и WADA статус
- FDA: Одобрено за диабет тип 2 (Mounjaro) и затлъстяване с ИТМ ≥30 или ≥27 със съпътстващо заболяване (Zepbound).
- EMA: Подобен път на одобрение.
- Класификация: Не е контролирано вещество.
- WADA (Световна антидопингова агенция): Всички агонисти на GLP-1 рецепторите бяха поставени в Програмата за мониторинг на WADA за 2024 г., сигнализирайки загриженост относно потенциална злоупотреба в спортове с категории тегло. Те все още не са забранени, но спортистите трябва да очакват засилен контрол и възможна бъдеща прекласификация.
- Застраховка: Засилващи се изисквания за предварително одобрение и контрол от страна на платците в САЩ поради високата цена и търсене. Употребата извън предписанията или за лица без затлъстяване често се отказва.
Компаундиран тирзепатид: Оценка на риска
Компаундирани или "биохакнати" версии, опитващи се да възпроизведат двойното инкретиново действие (обикновено чрез комбиниране на два отделни пептида като семаглутид + GIP), се различават фундаментално от фармацевтичния тирзепатид. Фармацевтичната версия е едномолекулен ко-агонист с проектирани съотношения на афинитет към рецепторите. Компаундираните смеси имат:
- Недоказани синергични съотношения.
- Неизвестна фармакокинетика.
- Липса на клинични данни при хора.
- Значителни рискове по отношение на чистотата и регулацията.
Анекдотични съобщения предполагат по-ниска ефикасност и по-променливи отговори. Фармацевтичният тирзепатид е силно предпочитан за всеки, който е сериозен относно резултатите и безопасността.
Проблемът с възвръщането на теглото
Данните от SURMOUNT-4 го направиха недвусмислено: спирането на тирзепатид води до значително възвръщане на теглото. Това не е провал на лекарството — то отразява патофизиологията на затлъстяването като хронично състояние с постоянни хормонални и неврологични адаптации, които се съпротивляват на поддържането на теглото.
За биохакинг общността това преформулира тирзепатид от "курс на лечение" в хронична терапия за повечето потребители. Изчислението на съотношението цена-полза се променя драстично, когато ангажиментът е потенциално за цял живот при $1,000+/месец.
Възникващи изследвания и бъдещи разработки
- SURMOUNT-MMO (сърдечно-съдови резултати при затлъстяване без диабет): Очаква се ~2027 г. Ще дефинира дългосрочната CV безопасност.
- SYNERGY-NASH (резолюция на NASH/MASH): Фаза 3, резултатите се очакват 2025–2026 г. Положителните резултати биха разширили значително показанията.
- Обструктивна сънна апнея: Активни изпитвания.
- Ретатрутид: GLP-1/GIP/Глюкагон три-агонист от следващо поколение в процес на разработка. Ранните данни предполагат дори по-голям потенциал за загуба на тегло.
- Орални формули: Орфорглипрон и други орални GLP-1 са в процес на разработка (времева линия 2025–2030 г.).
Ключови неотговорени въпроси
- Дали агонизмът на GIPR наистина запазва чистата маса при хората? Няма завършено RCT с DEXA, което да контролира упражненията. Това е критичната празнина за фитнес общността.
- Какви са 5-10 годишните ефекти от продължителното двойно инкретиново активиране? Неизвестни адаптивни рецепторни промени биха могли да намалят ефикасността или да предизвикат непредвидени ефекти.
- Има ли нетна полза при метаболитно здрави индивиди без затлъстяване? Този първичен случай на употреба за биохакинг е напълно неизследван. Рискът от загуба на чиста маса и странични ефекти може да надвиши пределните ползи в тази популация.
В обобщение
Тирзепатид е най-ефективният фармакологичен инструмент за загуба на тегло, наличен днес, подкрепен от мащабни, висококачествени данни от изпитвания при хора. Неговият двоен инкретинов механизъм осигурява 15–26% загуба на общо телесно тегло със значителни метаболитни подобрения в A1c, липиди, кръвно налягане и чернодробни мазнини. Той превъзхожда значимо семаглутид по отношение на загубата на тегло и гликемичния контрол.
Но това не е "хак" — това е хронично лекарство с реален профил на странични ефекти, висока финансова цена, почти сигурно възвръщане на теглото при спиране и критични празнини в знанията относно запазването на мускулите и дългосрочната безопасност. Доказателствата силно подкрепят употребата му при популации със затлъстяване и съпътстващи заболявания. За "оптимизационна" употреба от хора без затлъстяване, профилът риск-полза е неблагоприятен въз основа на настоящите данни. Използвайте го с отворени очи, комбинирайте го с тренировки с тежести и адекватен протеин, и не бъркайте клиничното превъзходство с безплатен обяд.