Ипаморелин: Селективен секретагог на растежния хормон
Механизъм, профил на селективност и практически протоколи
Въведение
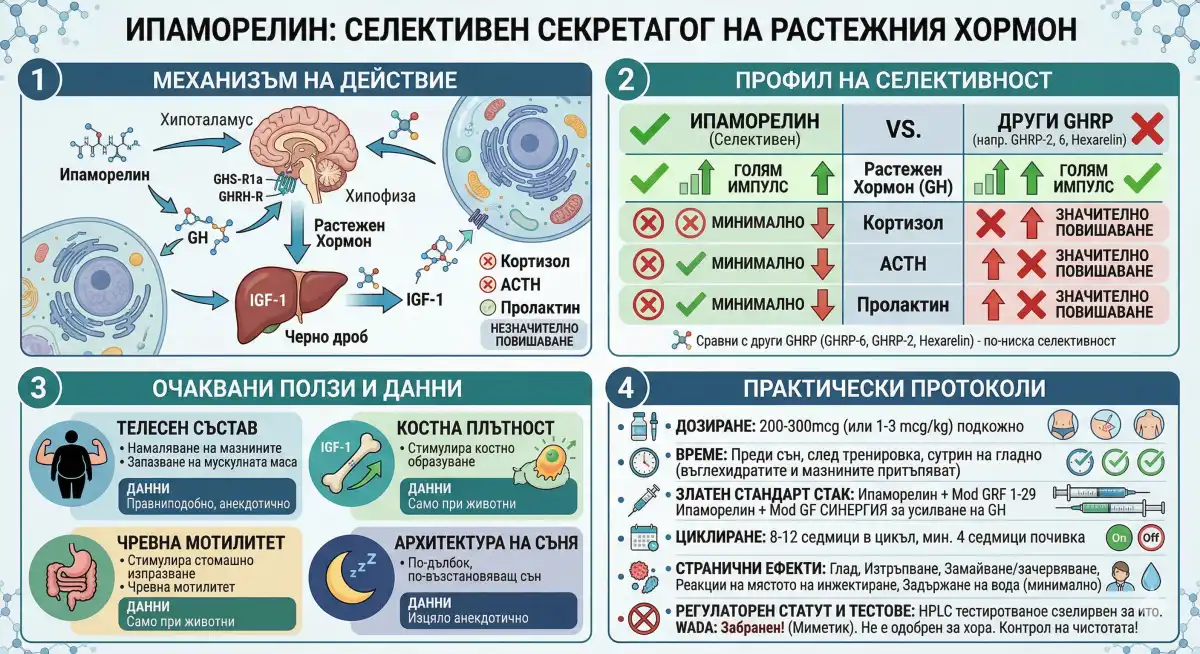
Ипаморелинът заема специфична ниша в пейзажа на секретагозите на растежния хормон (GHS): той е най-селективният наличен синтетичен GHS-R1a агонист, произвеждащ значими импулси на GH с минимални хормонални съпътстващи щети. За разлика от неговите братовчеди GHRP-6, GHRP-2 и Hexarelin — всички от които повличат със себе си кортизол, пролактин и ACTH — Ипаморелинът до голяма степен ограничава своята активност до соматотрофната ос. За потребителя на пептиди, който приоритизира чистия ендокринен профил пред суровата амплитуда на GH, тази селективност е цялото ценностно предложение.
Тази статия разбива молекулярния механизъм зад тази селективност, прави преглед на това какво всъщност подкрепят доказателствата (и къде не достигат), сравнява Ипаморелин директно срещу други GHRP-та и обхваща практическите протоколи, които са възникнали както от предклинични изследвания, така и от обширна употреба в общността.
Молекулярен механизъм: Как работи Ипаморелинът
Свързване с GHS-R1a и сигнализация надолу по веригата
Ипаморелинът е пентапептиден миметик на грелина — структурно съкратен в сравнение с ендогенния грелин (28 аминокиселини), но запазващ фармакофора, необходим за активиране на GHS-R1a. При свързване с GHS-R1a върху соматотрофите на предния дял на хипофизата, Ипаморелинът активира сигналната каскада Gq/11, предизвиквайки активиране на фосфолипаза С (PLC), генериране на инозитол трифосфат (IP3) и последваща вътреклетъчна мобилизация на калций. Този калциев поток е директният спусък за екзоцитоза на везикулите на GH.
Критичната разлика: съкратената структура на Ипаморелин означава, че му липсват молекулярните мотиви, които ангажират по-широки невроендокринни пътища. Той не активира значително хипоталамо-хипофизно-надбъбречната (ХХН) ос, нито стимулира лактотрофната секреция. Резултатът е освобождаване на GH без пиковете на кортизол, пролактин или ACTH, характерни за по-малко селективните GHRP-та.
Тази селективност е установена в основополагащата работа на Raun et al. (1998 г., Journal of Endocrinology), която демонстрира ефикасността на Ипаморелина за освобождаване на GH заедно с липсата на ефект върху ACTH, кортизол и пролактин при животински модели — профил, който е в ярък контраст с GHRP-6, тестван в същата парадигма.
Синергия с ендогенен GHRH
Ипаморелинът не действа изолирано в оста на GH. Агонизмът на GHS-R1a върху соматотрофите работи синергично с ендогенния хормон, освобождаващ растежен хормон (GHRH), който сигнализира чрез отделен рецептор (GHRH-R) върху същите клетки. Когато двата рецептора се активират едновременно, импулсът на GH се усилва отвъд това, което всеки от сигналите произвежда самостоятелно. Това е механистичната основа за комбиниране на Ипаморелин с екзогенни аналози на GHRH — двата агента подготвят соматотрофа чрез различни, но сближаващи се вътреклетъчни пътища.
Плато на зависимостта доза-отговор
Освобождаването на GH от Ипаморелин следва сигмоидална крива доза-отговор с ясна точка на насищане. След като заетостта на GHS-R1a достигне определен праг, допълнителният Ипаморелин не води до пропорционално увеличение на производството на GH. Този ефект на тавана е практически значим: той прави предозирането неефективно, а не опасно, и ограничава полезния диапазон на дозата до приблизително 1–3 mcg/kg телесно тегло (Raun et al., 1998 г., модели с плъхове). Данните за човешката фармакокинетика, подкрепящи тази крива, идват предимно от непубликувани корпоративни изпитвания, цитирани в обзорната литература — а не от рецензирани публикации.
Важна уговорка: Данните за дозата-отговор и селективността са предимно от проучвания върху животни (свине, плъхове). Директното характеризиране на дозата-отговор при хора в публикуваната, рецензирана литература е ограничено.
Проучвания за селективност: Anderson et al. и базата от доказателства
Сравнителният профил на селективност, който определя репутацията на Ипаморелин, се опира силно на Anderson et al. (2008 г., Journal of Endocrinological Investigation), което директно сравнява секретагозите на GH в модел на свине. Проучването потвърждава, че Ипаморелин произвежда мощно освобождаване на GH, сравнимо с други GHRP-та, докато кортизолът, пролактинът и ACTH остават на базови нива — профил, с който никое друго GHRP не може да се сравни.
Тези данни от животни, комбинирани с по-ранното характеризиране на Raun et al. и последователните анекдоти от общността в продължение на 15+ години, формират основата за твърдението за селективност. Въпреки това, трябва да се каже ясно: не съществува голямо, съвременно, рецензирано RCT при хора, което да потвърждава този профил на селективност при здрави възрастни, използващи протоколи, свързани с биохакинг. Доказателствата при хора се състоят от малки, по-стари корпоративни изпитвания (много от които не са публикувани изцяло) и екстраполация от силната предклинична основа.
Изследователски доказателства според приложението
Телесен състав
Очакваният механизъм — повишен пулсиращ GH, стимулиращ чернодробното производство на IGF-1, което от своя страна насърчава липолизата и запазването на чистата мускулна маса — е физиологично обоснован. Анекдотичните доклади на общността последователно описват скромна загуба на мазнини и подобрено възстановяване при цикли от 8–12 седмици. Въпреки това, публикуваните данни за телесния състав на човека от контролирани проучвания са оскъдни и стари, предимно от непубликувани корпоративни изследвания. Мащабът на ефекта при здрави, трениращи възрастни остава количествено неопределен в строгата литература.
Ниво на доказателства: Механистично правдоподобно, подкрепено от огромно количество анекдоти, но липсва съвременно потвърждение от човешки RCT.
Костна минерална плътност
Проучвания при оварийектомирани плъхове (стандартен модел за постменопаузална остеопороза) показват, че хроничното приложение на Ипаморелин повишава костната минерална плътност (BMD) и маркерите за костно образуване. Пътят е индиректен: Ипаморелин → импулси на GH → чернодробен IGF-1 → пролиферация на остеобласти и синтез на костен матрикс.
Ниво на доказателства: Само при животни. Няма широкомащабни, дългосрочни клинични проучвания при хора, които да оценяват промените в BMD с Ипаморелин. Пренасянето на тези открития към здрави хора — особено трениращи възрастни с нормални нива на естроген — изисква значителна екстраполация.
Чревна мотилитет
GHS-R1a се експресира в целия стомашно-чревен тракт. Агонизмът на Ипаморелин имитира установените прокинетични ефекти на грелина — стимулиране на изпразването на стомаха и чревната мотилитет чрез ентерични неврони и гладка мускулатура. Проучвания при животни с кучета и плъхове потвърждават този ефект.
Ниво на доказателства: Проучвания върху животни с механистична подкрепа от биологията на грелина. Данните при хора извън разработването на фармацевтични агонисти на грелина са изключително ограничени.
Архитектура на съня
Най-често цитираната субективна полза в докладите на общността е подобреното качество на съня — по-конкретно по-дълбок, по-възстановяващ сън, когато Ипаморелин се дозира преди лягане. Предложеният механизъм: екзогенният импулс на GH съвпада с първия естествен нощен скок на GH, а GH/IGF-1 участват в регулирането на бавновълновия сън.
Ниво на доказателства: Изцяло анекдотично. Не съществуват директни клинични проучвания на съня с Ипаморелин. Теоретичната връзка е правдоподобна, но непотвърдена, и плацебо ефектът не може да бъде изключен.
Сравнение на GHRP: Селективност срещу компромиси в ефективността
Параметър | Ипаморелин | GHRP-2 | GHRP-6 | Хексарелин |
|---|---|---|---|---|
Мощност на освобождаване на GH | Умерена | Висока (3–4× Ипаморелин) | Умерено-висока | Най-високата в класа |
Повишаване на кортизола | Пренебрежимо малко | Леко | Значително | Значително |
Повишаване на пролактина | Пренебрежимо малко | Леко | Значително | Значително |
Повишаване на ACTH | Пренебрежимо малко | Леко | Значително | Значително |
Стимулиране на глада | От леко до никакво | Леко-умерено | Силно изразено | Умерено |
Риск от десенсибилизация | Нисък (с циклиране) | Нисък-умерен | Умерен | Висок (бърза тахифилаксия) |
Практически случай на употреба | Чисто, устойчиво повишаване на GH; дълги цикли | По-силен анаболен сигнал; след тренировка | Покачване на маса (Bulking); стимулиране на апетита | Само за кратки диагностични импулси |
Ключов извод: Ипаморелинът жертва пиковата амплитуда на GH заради хормонална чистота. GHRP-2 е изборът за мощност с приемливи странични ефекти. GHRP-6 добавя стимулиране на апетита. Хексарелинът е твърде агресивен за продължителна употреба — той десенсибилизира в рамките на дни и рязко покачва кортизола/пролактина.
Практически протоколи
Дозиране
- Стандартна доза: 200–300 mcg на инжекция (приблизително 1–3 mcg/kg за повечето възрастни)
- Честота: 1–3 пъти дневно
- Приложение: Подкожна инжекция (корем, делтоиден мускул или бедро)
- Разтваряне: Лиофилизиран прах, разтворен с бактериостатична вода; съхранявайте в хладилник
Платото на дозата-отговор означава, че превишаването на 300 mcg на инжекция води до намаляваща възвръщаемост — вие насищате GHS-R1a без пропорционално увеличение на GH.
Прозорци за прием
- Преди сън (най-популярно): 200–300 mcg, 20–30 минути преди сън. Усилва първия нощен импулс на GH. Предпочита се състояние на гладно (въглехидратите и мазнините притъпяват освобождаването на GH).
- След тренировка: 200–300 mcg в рамките на 30 минути след тренировка. Насочва се към прозореца на GH, предизвикан от упражнения, за възстановяване.
- Сутрин на гладно: 200–300 mcg след събуждане, преди храна. Използва нощното гладуване за безпрепятствено освобождаване на GH.
За потребители, които дозират няколко пъти на ден, разстоянието между инжекциите от 3–4 часа с периоди на гладуване около всяка доза оптимизира пулсиращото производство на GH.
Златният стандартен стак: Ипаморелин + Mod GRF 1-29 (CJC-1295 no DAC)
Тази комбинация е най-широко препоръчваният протокол в пептидната общност и обосновката е механистично издържана:
- Ипаморелин активира GHS-R1a върху соматотрофите
- Mod GRF 1-29 активира GHRH-R върху същите соматотрофи
- Комбинирано: Синергично усилване на импулса на GH чрез два различни рецепторни пътя
Типичен протокол за стак:
- 100–200 mcg Ипаморелин + 100 mcg Mod GRF 1-29, смесени в една спринцовка
- 2–3 пъти дневно (преди сън е задължително; добавете сутрин и/или след тренировка)
Забележка: този стак се основава на теорията за рецепторна синергия и обширни експерименти в общността. Няма клинично изпитване за ефикасност при хора, което директно да сравнява стака с монотерапия или плацебо.
Циклиране
- В цикъл: 8–12 седмици
- Извън цикъл: минимум 4 седмици
- Обосновка: Предотвратява потенциалното низходящо регулиране на GHS-R1a и поддържа чувствителността към ендогенното сигнализиране на грелина
Дали хроничната циклична употреба (напр. години модели на 8 седмици прием/4 почивка) води до значима рецепторна десенсибилизация или притъпяване на оста на GH при хора е неизвестно — нито едно дългосрочно проучване при хора не се е занимавало с това.
Какво да очаквате от кръвните изследвания
- IGF-1: Очаквайте измеримо увеличение (често 20–50% над изходното ниво), откриваемо в рамките на 2–4 седмици. Това е основният обективен биомаркер.
- Нива на GH: Тестването на GH в даден момент е ненадеждно поради пулсиращата секреция. Ще е необходимо серийно вземане на проби.
- Кортизол/Пролактин: Трябва да останат на изходно ниво — това е потвърждението за селективност.
- Глюкоза на гладно/HbA1c: Наблюдавайте, тъй като GH има известен диабетогенен потенциал. Няма публикувани данни, които да определят количествено специфичното въздействие на Ипаморелин върху глюкозната хомеостаза при здрави потребители.
Странични ефекти
- Увеличаване на глада/апетита: Леко и преходно, обикновено след инжектиране. Много по-слабо изразено, отколкото при GHRP-6.
- Изтръпване/мравучкане: Докладвано е за периодично, преходно периферно изтръпване.
- Замайване/зачервяване: Кратък вазодилататорен ефект след инжекцията, по-често срещан в началото на употребата.
- Реакции на мястото на инжектиране: Стандартни за всеки подкожен пептид — зачервяване, леко дразнене.
- Задържане на вода: Минимално в сравнение с екзогенния GH или по-малко селективните GHRP-та.
Сериозни неблагоприятни ефекти не са систематично документирани, но липсата на дългосрочни данни за безопасността при хора означава, че продължават да съществуват неизвестни — особено по отношение на глюкозния метаболизъм и хроничните ефекти върху рецепторите.
Регулаторен и антидопингов статут
- Статут пред FDA: Не е одобрен за никакви показания. Продава се като "изследователски химикал" в САЩ — регулаторна сива зона за употреба от хора.
- Статут пред WADA: Забранен по всяко време. Всички агонисти на GHS-R попадат в списъка на забранените вещества на WADA като миметици на хормона, освобождаващ растежен хормон. Тестваните спортисти не могат да използват Ипаморелин.
- Снабдяване: Предлага се чрез специализирани аптеки (с рецепта в някои юрисдикции) и доставчици на изследователски пептиди. Чистотата и стерилността варират значително според доставчика — тестовете от трети страни (HPLC, масспектрометрия) са от съществено значение.
Отворени въпроси и пропуски в доказателствата
Три критични неизвестни определят границите на настоящите знания:
- Дългосрочна рецепторна десенсибилизация: Дали хроничната циклична употреба (>6 месеца) притъпява отговора на хипофизния GHS-R1a или потиска ендогенната пулсация на GH? Няма дългосрочни данни за хора.
- Въздействие върху глюкозния метаболизъм: GH е диабетогенен. Дали пулсиращото, селективно освобождаване на GH от Ипаморелин избягва влошаването на инсулиновата чувствителност във времето? Не са провеждани контролирани метаболитни проучвания.
- Пренасяне на откритията от животни: Костната плътност (модели на оварийектомирани плъхове), чревната мотилитет (модели на кучета/плъхове) и ефектите върху телесния състав не са валидирани в адекватни проучвания при хора.
В обобщение
Механизмът на Ипаморелина е надежден, неговият профил на селективност е добре подкрепен от предклинични данни, а профилът му на странични ефекти е наистина благоприятен в сравнение с всяко друго GHRP. Но интелектуалната честност изисква да се признае, че приложимите ползи — телесен състав, здраве на костите, сън, възстановяване — се опират на основата на данни от животни, непубликувани корпоративни изпитвания и обширни, но неконтролирани експерименти в общността.
За информирания потребител, който приема тези ограничения в доказателствата, Ипаморелинът предлага предсказуем инструмент с малко странични ефекти за подсилване на оста GH/IGF-1. Най-голямата му сила не е в създаването на най-големия пик на GH — GHRP-2 и Хексарелин печелят това състезание — а в осигуряването на устойчиво, физиологично моделирано повишаване на GH с минимален системен хормонален шум. Комбиниран с Mod GRF 1-29, дозиран консервативно, циклиран правилно и наблюдаван с кръвни изследвания, той остава най-практичният секретагог за потребители, които приоритизират дългосрочния хормонален баланс заедно с целите за физическо представяне.