ЧХГ: Гонадотропин за поддържане на тестостерона
Механизми, PCT протоколи и клинични доказателства
Въведение
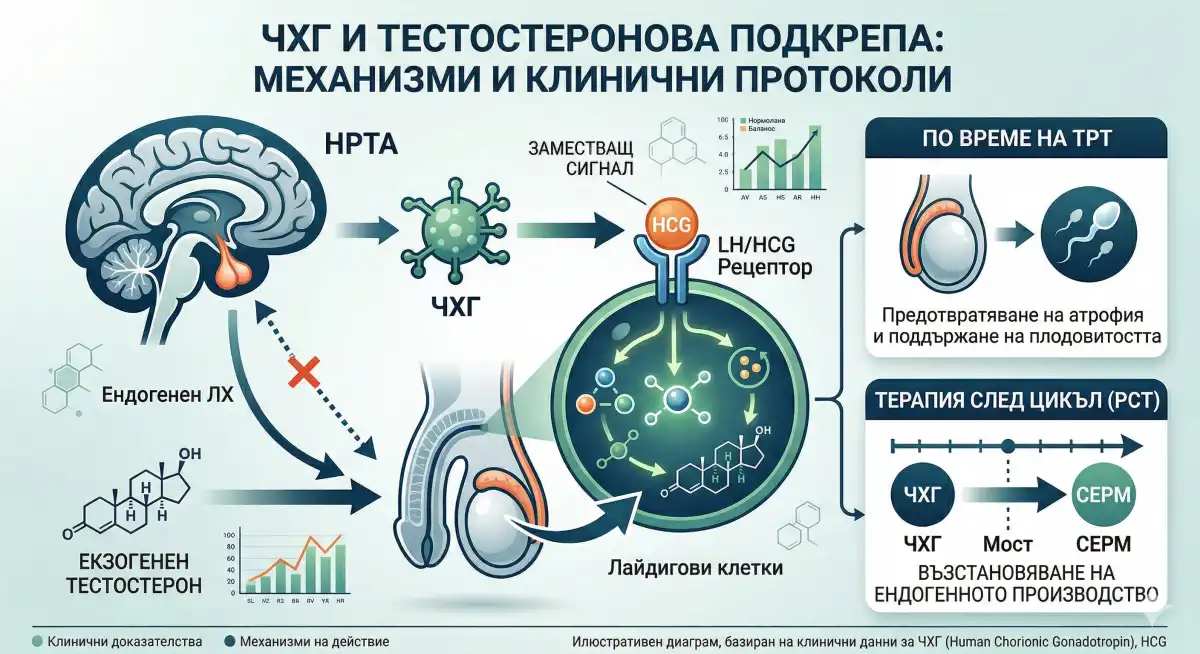
Човешкият хорионгонадотропин (ЧХГ) заема уникална позиция в инструментариума за спортни постижения и оптимизация. Той не е нито анаболен стероид, нито селективен модулатор на естрогенните рецептори — това е гликопротеинов хормон, който директно превзема същия рецептор като Лутеинизиращия хормон (ЛХ), принуждавайки лайдиговите клетки да произвеждат тестостерон, независимо от това какво прави хипофизата. За мъже на заместителна терапия с тестостерон (ТРТ) или анаболно-андрогенни стероиди (ААС), това прави ЧХГ основният фармакологичен инструмент за поддържане на функцията на тестисите в среда, където собственият ЛХ сигнал на тялото е заглушен.
Тази статия разглежда биохимията, оценява клиничните доказателства за всеки основен случай на употреба и предоставя практически насоки за протоколи, основани на това, което данните действително подкрепят — и къде не го правят.
Механизъм на действие: Агонизъм на ЛХ рецептора и стероидогенеза
Фармакологията на ЧХГ е ясна на рецепторно ниво. Той се свързва с рецептора на ЛХ/ХГ — G-протеин-свързан рецептор (GPCR), експресиран на повърхността на лайдиговите клетки в тестисите. Този рецептор не прави значима разлика между ендогенния ЛХ и екзогенния ЧХГ; и двете предизвикват една и съща вътреклетъчна сигнална каскада.
Сигналната каскада
- Свързване с рецептора → активиране на аденилат циклаза чрез Gs-протеиново свързване
- Производство на цАМФ (cAMP) → активиране на протеин киназа А (PKA)
- PKA фосфорилиране на стероидогенен остър регулаторен (StAR) протеин → транспорт на холестерол във вътрешната митохондриална мембрана (това е ограничаващата скоростта стъпка във всяка стероидогенеза)
- Регулация нагоре (Upregulation) на CYP17A1 и други стероидогенни ензими → превръщане на холестерола през прегненолон, DHEA и андростендион в тестостерон
Този път е добре описан както при хора, така и в in-vitro проучвания (Hall, 1999; Stocco, 2001). Ключовото прозрение: ЧХГ не просто "поддържа" производството на тестостерон — той директно задвижва цялата ензимна машинария от холестерола до тестостерона, заобикаляйки напълно нуждите от хипофизен ЛХ.
Фармакокинетично предимство пред ЛХ
ЧХГ има значително по-дълъг полуживот от ендогенния ЛХ (~24–36 часа срещу ~60 минути за ЛХ), поради остатъците от сиалова киселина в неговата бета субединица, които забавят бъбречния клирънс. Това означава, че една инжекция осигурява продължителна рецепторна стимулация за цял ден или повече — фармакокинетичен профил, който е едновременно предимство (удобно дозиране) и недостатък (непрекъснатото активиране на рецептора повдига опасения за десенсибилизация).
Вътретестикуларен тестостерон: Защо е важен
Серумният тестостерон ви дава информация за системния андрогенен статус. Вътретестикуларният тестостерон (ВТТ - ITT) ви дава информация за здравето на тестисите. Концентрациите на ВТТ са 50–100 пъти по-високи от серумните нива и този локален концентрационен градиент е от съществено значение за две неща:
- Сперматогенеза: Сертолиевите клетки се нуждаят от висок локален тестостерон, за да поддържат съзряването на зародишните клетки
- Обем на тестисите: Активността на лайдиговите клетки и целостта на семенните каналчета зависят от поддържания ВТТ
Когато екзогенният тестостерон потисне хипофизния ЛХ (което неизменно се случва), ВТТ се срива. Резултатът е атрофия на тестисите и нарушено или липсващо производство на сперма — често в рамките на седмици до месеци след започване на ТРТ или цикъл с ААС.
ЧХГ директно адресира това, като замества липсващия сигнал на ЛХ. Знаковото проучване на Coviello et al. (2004, Journal of Andrology) демонстрира, че съвместното приложение на ЧХГ с екзогенен тестостерон поддържа както нивата на ВТТ, така и сперматогенезата при здрави мъже — осигурявайки най-силното доказателство при хора за основната клинична полза от ЧХГ при ТРТ.
Случай на употреба 1: Поддържане на тестисите по време на ТРТ
Качество на доказателствата: Силно (клинични данни при хора)
Това е най-добре подкрепеното приложение на ЧХГ. Обосновката е превантивна: поддържане на функцията на тестисите по време на андрогенната терапия, вместо опити за възстановяването ѝ след нанасяне на щетите.
Стандартен протокол
Параметър | Препоръка |
|---|---|
Доза | 250–500 IU на инжекция |
Честота | 2–3 пъти седмично (напр. Пон/Сря/Пет или Пон/Чет) |
Път на въвеждане | Подкожно (SubQ - корем или бедро) |
Време | Едновременно с ТРТ от самото начало |
Седмичен общ прием | 500–1500 IU/седмично |
Подкожно (SubQ) срещу Интрамускулно (IM): Подкожното инжектиране вече е стандартна практика. Абсорбцията е малко по-бавна, но бионаличността е сравнима. SubQ е по-малко болезнено, използват се инсулинови спринцовки и води до по-малко усложнения на мястото на инжектиране.
Какво подкрепят доказателствата
- Запазване на обема на тестисите: Добре документирано в клинични проучвания
- Поддържане на сперматогенезата: Coviello et al. (2004) показват, че производството на сперма може да се поддържа, когато ЧХГ се прилага заедно с тестостерон
- Поддържане на ВТТ: Директните измервания потвърждават, че ЧХГ запазва вътретестикуларния градиент на тестостерона
Какво изисква наблюдение
ЧХГ стимулира тестикуларната ароматазна (CYP19) активност. Високият локален тестостеронов субстрат в комбинация с предизвиканата от ЧХГ регулация нагоре на ароматазата води до производството на значително количество естрадиол — не от периферна ароматизация (която ароматазният инхибитор би уловил), а от самите тестиси (Plymate et al., 1981). Това е фармакологично различен източник на естроген, който не може да бъде напълно контролиран от системни ароматазни инхибитори.
Кръвните изследвания трябва да включват естрадиол (чувствителен анализ) заедно с общ и свободен тестостерон най-малко на всеки 3–6 месеца.
Случай на употреба 2: Терапия след цикъл (PCT)
Качество на доказателствата: Слабо до умерено (механистичната обосновка е силна; липсват специфични данни за PCT при хора)
PCT (Терапия след цикъл) е мястото, където практиката в общността най-драстично изпреварва клиничните доказателства. Стандартният протокол "ЧХГ мост" (HCG bridge) е фармакологично рационален, но никога не е бил валидиран в контролирано проучване, специфично за спиране на ААС.
Логиката на ЧХГ моста
След цикъл с ААС, оста ХПТ (хипоталамус-хипофиза-тестиси) е потисната на всяко ниво:
- Хипоталамус: намалено производство на GnRH
- Хипофиза: потисната секреция на ЛХ и ФСХ
- Тестиси: атрофирали лайдигови клетки с намален стероидогенен капацитет
SERM (кломифен, енкломифен) действат на върха на тази ос, като блокират естроген-медиираната отрицателна обратна връзка в хипоталамуса/хипофизата, стимулирайки освобождаването на ЛХ/ФСХ. Но ако тестисите са силно атрофирали, освободеният ЛХ удря в нереагираща тъкан.
ЧХГ адресира дъното: той директно стимулира лайдиговите клетки да се "събудят", преди ендогенният ЛХ да се завърне. Идеята е последователно възстановяване — първо тестисите (ЧХГ), след това хипофизата (SERM).
Обществено приет стандартен PCT протокол
Фаза | Агент | Доза | Продължителност |
|---|---|---|---|
Мост (изчистване на естера) | ЧХГ | 250–500 IU през ден | 2–3 седмици |
Възстановяване | SERM (Предпочита се енкломифен) | 25 mg/ден | 4–6 седмици |
Критично фармакологично предупреждение: Самият ЧХГ осигурява отрицателна обратна връзка към оста хипоталамус-хипофиза. Той не "поддържа оста ХПТ будна" — той активно потиска производството на ЛХ от хипофизата, докато стимулира директно тестисите. Това означава, че ЧХГ трябва да бъде спрян преди започването на терапията със SERM, или в противен случай ще противодейства на механизма на SERM. Този нюанс често се разбира погрешно.
PCT протоколи с високи дози: Предупреждение
По-старите протоколи изискваха агресивно дозиране на ЧХГ по време на PCT — 1500–5000 IU многократно седмично. Тези дози са екстраполирани от проучвания за индукция на плодовитостта, а не от възстановяване след ААС. Доказателства от Smals et al. (1980) и животински модели (Huhtaniemi et al., 1980) показват, че продължителната супрафизиологична стимулация на ЛХ рецептора причинява десенсибилизация на рецептора — разединяване на рецептора от неговия G-протеин, интернализация на рецептора и намалена експресия на стероидогенни ензими.
Прагът доза-продължителност за клинично значима десенсибилизация при хора, използващи съвременни протоколи с по-ниски дози (250–500 IU, 2–3 пъти/седмично), остава неопределен — това е един от най-важните въпроси без отговор в тази област.
Случай на употреба 3: Запазване на плодовитостта по време на ТРТ
Качество на доказателствата: Умерено до силно (съществуват данни при хора, но оптималните протоколи са недостатъчно проучени)
За мъже на ТРТ, които искат да запазят възможността за бащинство, ЧХГ е от съществено значение. Без него екзогенният тестостерон действа като мъжки контрацептив — потискането на ЛХ/ФСХ води до олигоспермия или азооспермия при значителна част от мъжете в рамките на 6–12 месеца.
ЧХГ поддържа ВТТ, достатъчен за базова сперматогенеза. Има обаче едно важно ограничение:
ЧХГ няма ФСХ активност. Фоликулостимулиращият хормон е критичен за сперматогониалната пролиферация и поддръжката на сертолиевите клетки. ЧХГ самостоятелно поддържа, но може да не оптимизира производството на сперма, особено при мъже с вече компрометирани параметри на семенната течност.
За мъже с лоши резултати от спермограмата въпреки употребата на ЧХГ, добавянето на ФСХ — чрез ЧМГ (Човешки менопаузален гонадотропин - HMG) или рекомбинантен ФСХ — е следващата клинична стъпка.
ЧХГ срещу ЧМГ: Кога да ескалираме
Характеристика | ЧХГ | ЧМГ |
|---|---|---|
ЛХ активност | Да (директен агонист) | Да (съдържа ЛХ) |
ФСХ активност | Не | Да (обикновено 75 IU FSH на флакон) |
Полуживот | ~24–36 часа | ~60 минути (ЛХ компонент) |
Основна употреба | Поддържане на тестостерон/ВТТ | Пълно възстановяване на сперматогенезата |
Цена | По-ниска | Значително по-висока |
Кога да се използва | Подкрепа при ТРТ, леко потискане | Тежка олигоспермия/азооспермия, активен опит за зачеване |
Това разграничение — ЧХГ за поддръжка, ЧМГ/rFSH за спасяване — често се пренебрегва в биохакинг средите, където ЧХГ понякога се третира като цялостно решение за плодовитост.
Случай на употреба 4: Монотерапия с ЧХГ
Качество на доказателствата: Слабо (само малки, краткосрочни проучвания)
Монотерапията с ЧХГ — използването само на ЧХГ за лечение на хипогонадизъм без екзогенен тестостерон — има теоретична привлекателност: стимулира ендогенното производство, запазва плодовитостта и избягва спирането на функцията на тестисите. На практика обаче доказателствата са неубедителни.
Малки проучвания показват, че монотерапията с ЧХГ може да повиши тестостерона до средни стойности при мъже с вторичен хипогонадизъм. Въпреки това:
- Постигнатите нива на тестостерон обикновено са скромни и непоследователни
- Изискват се чести инжекции (3–7 пъти седмично в някои протоколи)
- Цената е значително по-висока от тази на тестостерон ципионат/енантат
- Повишаването на естрадиола е пропорционално по-голямо, отколкото само при ТРТ
- Дългосрочни данни практически липсват
Оценката на съотношението риск-полза е неблагоприятна за повечето мъже със симптоматичен хипогонадизъм. ТРТ или SERM (по-специално енкломифен) са по-ефективни, практични и по-добре проучени опции на първи избор. Монотерапията с ЧХГ заема тясна ниша за мъже, които отказват както екзогенен тестостерон, така и орални SERM.
Управление на естрогена: Проблемът с вътретестикуларната ароматизация
ЧХГ повишава естрадиола чрез механизъм, различен от периферната ароматизация, която се случва при екзогенния тестостерон. ЧХГ регулира нагоре тестикуларната ароматазна (CYP19) активност и едновременно наводнява лайдиговите клетки с тестостеронов субстрат — комбинацията произвежда значителен вътретестикуларен естрадиол, който навлиза в системното кръвообращение.
Това има практическо значение:
- Анастрозол/летрозол (системни АИ) могат непълно да контролират предизвикания от ЧХГ естрадиол, тъй като източникът е вътретестикуларен
- Реакцията на дозата е нелинейна: добавянето на 500 IU ЧХГ към ТРТ може да повиши E2 диспропорционално повече от съответното увеличение на тестостерона
- Симптоми, които да наблюдавате: задържане на вода, повишаване на кръвното налягане, промени в настроението, чувствителност на зърната
Решението за добавяне на АИ (ароматазен инхибитор) трябва да се ръководи от симптомите и кръвните изследвания, а не профилактично. Свръхпотискането на естрадиола носи свои собствени рискове (болки в ставите, нарушаване на липидния профил, загуба на костна плътност).
Протокол за наблюдение на кръвните показатели
Минимален панел за мъже, използващи ЧХГ (със или без ТРТ):
Маркер | Защо | Честота |
|---|---|---|
Общ тестостерон | Оценка на ефикасността | На всеки 3–6 месеца |
Свободен тестостерон | Статус на бионаличен андроген | На всеки 3–6 месеца |
Естрадиол (чувствителен) | Наблюдение на ароматизацията, предизвикана от ЧХГ | На всеки 3–6 месеца; по-често при започване |
ЛХ / ФСХ | Оценка на потискането на хипофизата (очаква се да е близо до нула при ТРТ+ЧХГ) | Базово (в началото), след това при нужда |
Хематокрит / Хемоглобин | Риск от полицитемия (главно от тестостерон) | На всеки 6 месеца |
PSA (ПСА) | Скрининг на простатата | Ежегодно (над 40 г.) |
Спермограма | Ако плодовитостта е цел | При нужда |
Регулаторен и антидопингов статус
- FDA (Агенция за контрол на храните и лекарствата на САЩ): ЧХГ е лекарство по лекарско предписание, одобрено за хипогонадизъм и плодовитост. Употребата извън предписанията (off-label) за подкрепа на ТРТ е често срещана, но не е официално индикирана.
- WADA (Световна антидопингова агенция): ЧХГ е забранен по всяко време за мъже спортисти (S2: Пептидни хормони, растежни фактори, сродни вещества). Той се открива чрез уринен имуноанализ. Употребата по време на състезание или извън състезание представлява нарушение на антидопинговите правила.
- Снабдяване: В САЩ, Обединеното кралство и ЕС, ЧХГ изисква рецепта. Пейзажът на компаундинг аптеките (аптеки, които приготвят лекарства по поръчка) се промени след действията по правоприлагане на FDA през 2020 г. върху определени продукти с ЧХГ, тласкайки някои потребители към чуждестранни или сиви пазари с променливо качество.
Изследователски хоризонти и бъдещи насоки
Няколко области на активно изследване могат да прекроят употребата на ЧХГ през следващите 3–5 години:
- Протоколи с микродозиране (100–150 IU дневно), опитващи се да имитират физиологичната пулсация на ЛХ, набират популярност в биохакинг общностите, с анекдотични съобщения за намалено превръщане в естроген и запазен обем на тестисите. За тях липсва клинично валидиране.
- Оптимизираните ТРТ протоколи за плодовитост се насочват към по-ниско и по-често дозиране (150–300 IU през ден), за да се сведат до минимум естрогенните пикове.
- Следващо поколение модулатори на ЛХ рецепторите с по-благоприятна фармакокинетика в крайна сметка могат да предложат алтернативи на ЧХГ.
- Възходът на енкломифена като основен агент за PCT може да намали ролята на ЧХГ във възстановяването след цикъл, въпреки че ролята му по време на активна употреба на ТРТ/ААС остава неоспорима.
- Очакват се дългосрочни данни за кардиометаболитната безопасност и безопасността на простатата за ТРТ+ЧХГ спрямо само ТРТ в рамките на 3–5 години.
Ключови изводи
- Най-силната база от доказателства за ЧХГ е за превантивна употреба по време на ТРТ — запазване на обема на тестисите, ВТТ и потенциала за плодовитост
- Той работи чрез директен агонизъм на ЛХ рецептора, задвижвайки пълната стероидогенна каскада от холестерола до тестостерона
- Той не запазва функцията на оста ХПТ на хипоталамо-хипофизарно ниво — той я потиска чрез отрицателна обратна връзка, докато стимулира тестисите
- 250–500 IU, 2–3 пъти/седмично SubQ е настоящият стандарт за подкрепа при ТРТ
- При PCT го използвайте като кратък мост преди SERM, а не като самостоятелен агент за възстановяване
- Следете естрадиола отблизо — ЧХГ стимулира вътретестикуларната ароматизация, която системните АИ може да не контролират напълно
- ЧХГ не е цялостно решение за плодовитост — липсва му ФСХ активност; добавете ЧМГ или rFSH, ако параметрите на спермограмата са лоши
- Монотерапията е субоптимална за повечето мъже със симптоматичен хипогонадизъм
- Рискът от десенсибилизация съществува, но точният праг доза-продължителност в съвременните протоколи е неопределен