Глутатион: Главният антиоксидант
Клетъчни защитни механизми, изчерпване и суплементация
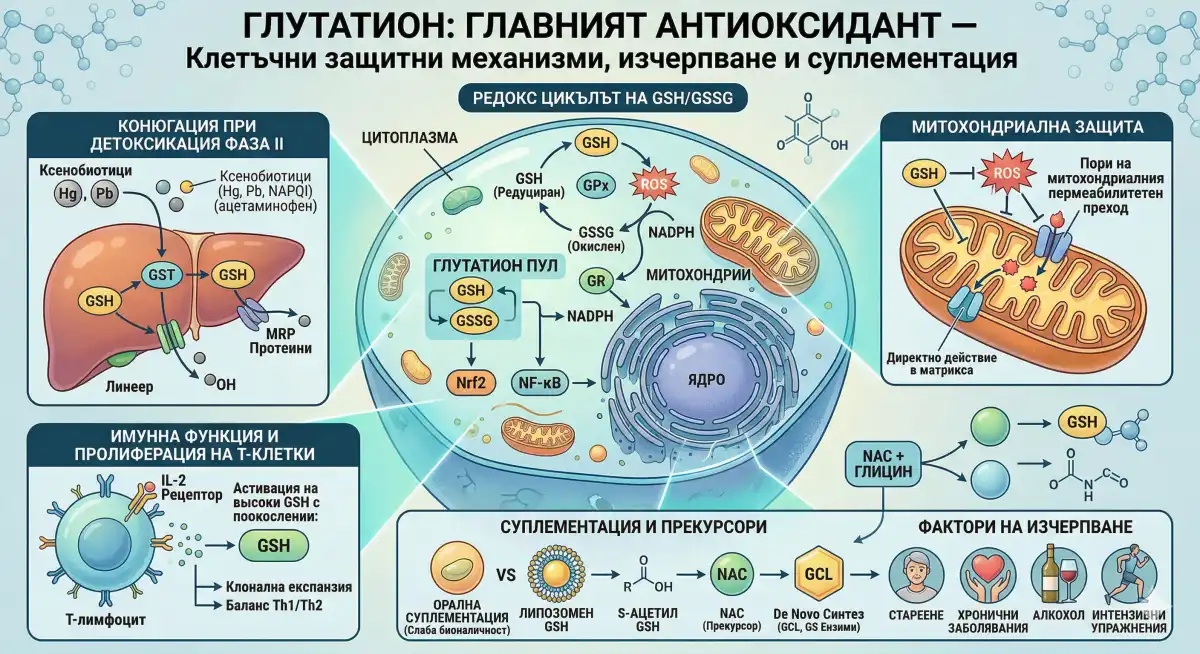
Биохимията, която трябва да разберете
Глутатионът (GSH) е трипептид — глутамат, цистеин, глицин — и най-изобилният вътреклетъчен антиоксидант във всяка клетка на човешкото тяло. Той не е просто молекула, която "почиства свободните радикали". GSH функционира като централен регулаторен възел в клетъчната редокс сигнализация, детоксикацията, имунната модулация и контрола на апоптозата. Ако ви е грижа за оптимизирането на клетъчната функция, разбирането на биохимията на GSH е абсолютно задължително.
Редокс цикълът на GSH/GSSG
Основният механизъм: GSH дарява електрони за неутрализиране на реактивните кислородни видове (ROS) — включително водороден пероксид, генериран от митохондриалното дишане, възпалителни каскади и метаболизма на ксенобиотиците. Тази реакция се катализира от глутатион пероксидаза (GPx), превръщайки редуцирания GSH в неговия окислен димер, GSSG.
Съотношението GSH/GSSG не е просто метрика за отпадъчни продукти. То функционира като първичен редокс сигнал, който директно модулира:
- Активността на NF-κB — главният транскрипционен фактор за възпалението, който става по-активен при оксидативни условия (по-ниско съотношение GSH/GSSG).
- Пътят Nrf2 — елементът на антиоксидантния отговор на клетката, активиран при определени електрофилни и редокс стресове за регулиране на производството на ендогенни антиоксидантни ензими.
- Киназата ASK1 — ключова киназа, регулираща сигнала за апоптоза, която се инхибира от редуцирания GSH; когато GSH спадне, ASK1 се активира, тласкайки клетката към програмирана смърт.
- Порите на митохондриалния пермеабилитетен преход — изчерпването на GSH в митохондриите може да предизвика отваряне на порите, освобождаване на цитохром c и апоптоза.
Ето защо изчерпването на GSH не е просто "оксидативен стрес" — то е промяна във фундаменталното сигнализиращо състояние на клетката, засягащо пролиферацията, възпалителния тонус и решенията за оцеляване (Forman et al., 2009).
Конюгация при детоксикация Фаза II
GSH е необходим субстрат за Фаза II на детоксикацията, главно в черния дроб и бъбреците. Глутатион S-трансферазите (GST) катализират конюгацията на GSH към електрофилни токсини — лекарства, замърсители, тежки метали и ендогенни реактивни алдехиди като 4-хидроксиноненал (продукт на липидната пероксидация). Полученият GSH-конюгат е водоразтворим и активно се изнася от клетките чрез протеини, свързани с мултилекарствената резистентност (MRP), за жлъчна или уринарна екскреция.
Това не е само на теория. NAC — пролекарство на цистеина, което възстановява GSH — е стандартното лечение при предозиране с ацетаминофен именно защото възстановява чернодробния резерв на GSH, необходим за Фаза II конюгация на токсичния метаболит NAPQI. Този път е валидиран от десетилетия клинична употреба при хора.
Имунна функция: По-сложно от "подсилва имунитета"
Активирането на лимфоцитите и клоналната експанзия изискват редуцираща вътреклетъчна среда, а GSH е основният детерминант за тази среда. Когато вътреклетъчният GSH спадне:
- Сигнализирането на IL-2 рецептора е нарушено, което намалява пролиферацията на Т-клетките.
- Балансът на Т-хелперните клетки се измества от Th1 (клетъчно-медиирани) към Th2 (хуморални/движени от антитела) цитокинови профили.
- Производството на провъзпалителни цитокини от макрофагите (TNF-α) може да се увеличи.
Това е обстойно проучвано в контекста на ХИВ/СПИН, където системното изчерпване на GSH корелира с прогресията на заболяването и нарушеното имунно възстановяване (Peterson et al., 1998; Dröge & Breitkreutz, 2000). Доказателствата за тези имунни механизми са предимно от ин витро и проучвания върху животни, като клиничните данни са предимно от имунокомпрометирани популации — екстраполацията към здрави индивиди изисква повишено внимание.
Критичен нюанс: Имунните ефекти на GSH са двуфазни и зависещи от контекста. Дефицитът нарушава функцията, но прекомерното повишаване в специфични компартменти може да изкриви имунните отговори непредсказуемо. Анекдотични доклади в биохакерските общности описват автоимунни обостряния при протоколи с високи дози GSH. Това е реално съображение за всеки с автоимунни заболявания.
Какво изчерпва глутатиона
Нуждата от GSH се увеличава — и резервът може да бъде изпреварен — при следните условия:
- Стареене — експресията на GCL (ензимът, ограничаващ скоростта на синтеза на GSH) намалява с възрастта; при по-възрастните хора постоянно се наблюдават по-ниски нива на тъканен GSH.
- Хронични заболявания — ХИВ, ХОББ, чернодробни заболявания, диабет и невродегенеративни състояния се характеризират с документирано изчерпване на GSH.
- Алкохол — метаболизмът на етанола генерира ацеталдехид, който директно се конюгира с GSH и изчерпва чернодробния резерв.
- Тежки метали — живакът, оловото, арсенът и кадмият директно свързват GSH и го изчерпват чрез конюгация и екскреция.
- Интензивни упражнения — тренировките с голям обем увеличават производството на митохондриални ROS, като остро изчерпват мускулния и системния GSH.
- Токсини от околната среда — пестицидите, разтворителите и замърсяването на въздуха консумират GSH чрез Фаза II конюгация.
Проблемът с оралната бионаличност
Това е централното предизвикателство при суплементацията с GSH и причината стандартните орални капсули с глутатион до голяма степен да са загуба на пари за системни цели.
GSH е трипептид. Когато го погълнете, чревната гама-глутамилтранспептидаза (GGT) и дипептидазите го хидролизират до съставните му аминокиселини — глутамат, цистеин и глицин — преди да достигне до системното кръвообращение. Непокътнатият GSH има слаба пропускливост през чревната мембрана. Фармакокинетични проучвания при хора са потвърдили минимални увеличения на плазмения или тъканния GSH от стандартната орална суплементация (Witschi et al., 1992; Allen & Bradley, 2011).
Ключово прозрение: Проблемът с оралната бионаличност е проблем специално за постигане на системни увеличения на непокътнат GSH. За поддържане на чернодробния GSH — където хидролизираните аминокиселини се сглобяват отново чрез синтез de novo — оралните прекурсори са ефективни и добре доказани. Това разграничение е важно за съставянето на протокола.
Пътища на приложение и решения за доставка
Сравнение на методите за доставка на GSH
Метод | Механизъм | Системно увеличение на GSH | Ниво на доказателства | Цена | Практичност |
|---|---|---|---|---|---|
Стандартен орален GSH | Хидролизира се до аминокиселини в червата | Минимално (в плазмата) | Високо (потвърдена слаба бионаличност) | Ниска | Лесно |
NAC (прекурсор) | Пролекарство на цистеин → чернодробен de novo синтез | Силно (чернодробно); умерено (системно) | Силно (десетилетия данни при хора) | Ниска | Лесно |
Глицин + NAC (GlyNAC) | Осигурява и двата ограничаващи скоростта прекурсора | Силно (чернодробни и системни маркери) | Умерено (нововъзникващи рандомизирани контролирани проучвания при хора) | Ниска | Лесно |
Липозомен GSH | Фосфолипидното капсулиране предпазва от хидролиза | Умерено-добро (в плазмата и левкоцитите) | Умерено (фармакокинетични проучвания при хора, напр. Sinha et al., 2018) | Висока | Лесно |
S-ацетил GSH | Ацетилната група предотвратява хидролизата; разцепва се вътреклетъчно | Умерено-добро (вътреклетъчно, в левкоцитите) | Ограничено (появяват се фармакокинетични данни при хора) | Висока | Лесно |
Интравенозен (IV) GSH | Директна доставка в кръвообращението | Най-високи пикови плазмени нива | Умерено (данни от клинична употреба) | Много висока | Изисква медицинско наблюдение |
Суроватъчен протеин | Богат на цистеин и цистин за de novo синтез | Умерено (поддържа чернодробния резерв) | Умерено (проучвания при хора) | Ниска-умерена | Лесно |
NAC: Работният прекурсор
N-ацетилцистеинът е пролекарство на цистеина и най-подкрепената с доказателства интервенция за повишаване на вътреклетъчния GSH. Абсорбира се добре орално, доставя цистеин (ограничаващата скоростта аминокиселина за синтеза на GSH) и има десетилетия данни за безопасността и ефикасността при хора — предимно за възстановяване на чернодробния GSH.
Стандартно дозиране: 600–1800 mg/ден в разделени дози. Протоколът от 600 mg два пъти дневно се понася добре и се използва широко. По-високи дози (до 1800 mg/ден) се използват в клинични условия за специфични показания.
Ограничения: NAC работи чрез синтез de novo, което изисква адекватна ензимна активност на GCL. При състояния, при които GCL е понижен (тежко чернодробно заболяване, напреднало стареене), самото снабдяване с прекурсори може да не възстанови напълно резерва от GSH. NAC може също да причини стомашно-чревен дискомфорт при по-високи дози.
GlyNAC: Комбинираният протокол
Скорошни изследвания подчертават, че глицинът — а не само цистеинът — може да бъде ограничаващ фактор за синтеза на GSH, особено при по-възрастни хора. Комбинацията GlyNAC (глицин + NAC) показва обещаващи резултати в проучвания при хора за повишаване на GSH и подобряване на маркерите за оксидативен стрес при застаряващо население. Практичен орален комбиниран подход.
Обичайно дозиране: NAC 600 mg + Глицин 1–3 g, два пъти дневно.
Липозомен GSH
Липозомното капсулиране обгръща редуцирания GSH във фосфолипидни бислоеве, предпазвайки го от чревна хидролиза и потенциално позволявайки абсорбиране в непокътнат вид. Фармакокинетичните данни при хора (Sinha et al., 2018) показват значими увеличения на нивата на GSH в плазмата и левкоцитите в сравнение със стандартния орален GSH.
Обичайно дозиране: 250–500 mg/ден. Качеството варира значително между производителите — тестването от трети страни и правилното съхранение в хладилна верига са от съществено значение.
Предупреждение: Въпреки че фармакокинетичните данни са обещаващи, мащабните проучвания при хора, демонстриращи функционални резултати (подобряване на имунитета, възстановяване, детокс маркери) специално от липозомен GSH, са все още ограничени.
S-ацетил глутатион
Ацетилната група върху цистеиновия остатък предотвратява хидролизата в червата и прави молекулата пропусклива за клетките. Веднъж вътре в клетката, естеразите отцепват ацетилната група, освобождавайки редуциран GSH. Ограничените фармакокинетични данни при хора предполагат значително по-добра орална бионаличност от стандартния GSH и способността да се повишава вътреклетъчният GSH в левкоцитите.
Обичайно дозиране: 200–400 mg/ден на гладно.
Интравенозен (IV) глутатион
Интравенозното приложение постига най-високите и най-незабавни скокове на плазмения GSH. Използва се клинично в някои заведения за интегративна медицина за:
- Допълнителна подкрепа по време на протоколи за хелатиране при натоварване с тежки метали.
- Подпомагане на пациенти, подложени на химиотерапия.
- Неврологични заболявания (Паркинсон — ограничени доказателства).
Обичайно клинично дозиране: 600–2400 mg на сесия, 1–3 пъти седмично.
Това е медицинска процедура, изискваща наблюдение. Не е ежедневен инструмент за самооптимизация.
Клинични доказателства по случаи на употреба
Подпомагане на детоксикацията на черния дроб
Доказателства: Силни. NAC е златен стандарт за лечение на токсичност от ацетаминофен чрез възстановяване на чернодробния GSH. Отвъд острото отравяне, добавянето на прекурсори надеждно поддържа капацитета за конюгация от Фаза II в черния дроб. Това е приложението с най-много доказателства.
Имунна функция (ХИВ, имунокомпрометирани)
Доказателства: Умерени. Изчерпването на GSH е добре документирано при ХИВ и корелира с прогресирането на заболяването. Суплементацията (предимно NAC) е показала ползи в някои проучвания за имунните маркери. Данните при здрави популации са ограничени — имунните ползи са най-подходящи за тези с документирано изчерпване.
Изсветляване на кожата
Доказателства: Слаби. Механизмът е правдоподобен — GSH инхибира тирозиназата и измества производството на меланин към по-светлия феомеланин вместо към еумеланин (Villarama & Maibach, 2005). Съществуващите проучвания при хора обаче са малки, често отворени и с кратка продължителност. Дерматологичните данни не подкрепят уверени твърдения. Съотношението риск-полза за козметична употреба е класифицирано като недостатъчни данни, особено предвид опасенията относно нерегулираното качество на продуктите.
Спортно възстановяване
Доказателства: Смесени. Прекурсорите на GSH (NAC, суроватъчен протеин) могат да намалят маркерите за оксидативен стрес и възпаление (CRP, CK) след тренировка. Въпреки това, директният превод към измеримо повишаване на производителността или ускорено възстановяване при добре хранени, тренирани спортисти е слаб. Дали директната доставка на GSH (липозомен, ацетил) осигурява предимство пред адекватния прием на прекурсори при тази популация остава отворен въпрос без преки сравнителни проучвания.
Подкрепа при хелатиране на тежки метали
Доказателства: Само поддържаща роля. GSH улеснява жлъчната екскреция на метали като живак чрез Фаза II конюгация. Той не е първичен хелатор — DMPS и DMSA са утвърдените хелатиращи агенти. GSH служи като адювант в структурирани протоколи за хелатиране под медицинско наблюдение. Използван самостоятелно при значителна токсичност с тежки метали, той дава фалшиво чувство за сигурност и може да преразпредели металите.
Практически протоколи
Основен стак (Рентабилен, базиран на доказателства)
- NAC: 600 mg два пъти дневно.
- Глицин: 2–3 g два пъти дневно.
- Витамин C: 500–1000 mg/ден (рециклира окисления GSH обратно в редуцирана форма).
- Суроватъчен протеин: 20–30 g/ден (допълнителен източник на цистеин).
Това покрива подкрепата за чернодробния GSH със силни доказателства. Подходящо като база за повечето потребители.
Разширен системен протокол
Добавете към основния стак:
- Липозомен GSH: 250–500 mg/ден, или
- S-ацетил GSH: 200–400 mg/ден на гладно.
Цел: системна антиоксидантна подкрепа извън черния дроб. Обмислете го за периоди на високо токсично натоварване, интензивни тренировъчни блокове или възстановяване след заболяване.
Стратегия за циклиране
Най-практичният протокол може да включва циклиране между прекурсори и директна доставка на GSH:
- Седмици 1–4: Само прекурсори (NAC + Глицин + Витамин C) — поддържа и стимулира ендогенния синтез.
- Седмици 5–6: Добавете липозомен или S-ацетил GSH за целенасочен системен тласък.
- Седмица 7: Спрете директния GSH; поддържайте прекурсорите.
Обосновка: Избягва теоретичния риск от потискане на GCL/GS ензимите, отговорни за de novo синтеза, при хронична суплементация с директен GSH. Това опасение се основава на фармакодинамична логика и обществена практика, а не на потвърдени данни при хора — но предпазният подход не струва нищо.
Комбиниране с индуктори на Nrf2
Сулфорафанът (от екстракт от семена на броколи, ~10–20 mg/ден) активира пътя Nrf2, като регулира нагоре производството на ендогенни антиоксидантни ензими, включително GCL. Комбинирането с прекурсори на GSH адресира както страната на предлагането (субстрат), така и страната на търсенето (ензимна активност) на уравнението.
Съображения за безопасност
- NAC в стандартни дози (<1800 mg/ден): Понася се добре. Стомашно-чревният дискомфорт е основният страничен ефект. Редки анафилактоидни реакции са възможни при интравенозен NAC.
- Дългосрочен прием на високи дози NAC: Не е напълно характеризиран за безопасност. Някои данни от животни пораждат опасения за потенциални прооксидантни ефекти при много високи дози.
- Форми на директен GSH (липозомен, ацетил): Не са докладвани сериозни неблагоприятни ефекти при стандартни дози. Данните за дългосрочна безопасност са ограничени.
- Интравенозен (IV) GSH: Като цяло се понася добре, но изисква медицинско наблюдение. Възможни са редки алергични реакции.
- Автоимунни заболявания: Подхождайте с повишено внимание. Имунната модулация на GSH е сложна и двупосочна. Суплементацията би могла теоретично да влоши Th2-управлявани или медиирани от антитела състояния. Консултирайте се с компетентен специалист.
- Качество на продукта: Липозомните GSH продукти варират изключително много по качество. Цялостта на фосфолипидите се влошава с топлината и времето. Избирайте продукти с тестове от трети страни и подходящи условия за съхранение.
Регулаторен статут
- WADA (Световна антидопингова агенция): Глутатионът не е забранен. Разрешен е по време на и извън състезания.
- САЩ: GSH, NAC и прекурсорите се продават като хранителни добавки под регулацията на FDA (не като лекарства). Качеството на липозомните продукти не се проверява строго.
- ЕС: NAC се счита за разрешено лекарство за муколитична употреба от EMA. Статутът на добавка варира в зависимост от държавата.
На какво още трябва да отговорят изследванията
- Дали хроничната суплементация с директен GSH потиска ензимите за ендогенен синтез (GCL, GS) при хората? Това определя дали циклирането е интелигентна предпазна мярка или ненужно усложнение.
- Дали директната доставка на GSH превъзхожда адекватния прием на прекурсори за спортно възстановяване при добре хранени спортисти? Ако не, надценката в цената на липозомните/ацетилните форми е неоправдана за тази популация.
- Какъв е точният профил на риск/полза при активно автоимунно заболяване? Имунологичната сложност на GSH означава, че общите препоръки са преждевременни.
Клиничните изпитвания, тестващи липозомен и S-ацетил GSH за специфични състояния — Дълъг COVID, невродегенеративни заболявания, автоимунна модулация — се очаква да се размножат през 2025–2027 г., преминавайки отвъд фармакокинетичните проучвания към функционални резултати. Взаимодействието между суплементацията с GSH, чревния микробиом и системното възпаление е друга граница, която вероятно ще види значителна изследователска дейност до 2030 г.
В обобщение
Биохимията на GSH е непоклатима. Молекулата наистина е централна за клетъчната защита, детоксикацията и имунната регулация. Пейзажът на интервенциите обаче е стратифициран: NAC и комбинациите от прекурсори са добре доказани, рентабилни и достатъчни за чернодробна и основна подкрепа. Новите форми на доставка (липозомни, S-ацетил) показват реално фармакокинетично обещание за системно повишаване, но им липсват мащабни данни за резултатите, които да оправдаят по-високата им цена за повечето потребители. Започнете с основния стак. Добавяйте усъвършенствани форми за доставка стратегически и циклично. Не използвайте GSH като самостоятелен хелатор на тежки метали. И ако имате автоимунни заболявания, продължете с информирано внимание — това не е просто молекула на принципа "колкото повече, толкова по-добре".